Selon les dernières données de
l'Organisation mondiale de la santé, plus de 80 maladies auto-immunes sont
connues et affectent entre 3 et 7% de la population occidentale.
Dans cette large proportion, ces
troubles touchent de manière disproportionnée les femmes, qui représentent près
de 80% des cas. Elles les affectent souvent à un âge fertile et deviennent donc
une complication pour la grossesse. Les raisons de cette situation inégalitaire
ne sont toujours pas très bien comprises par les médecins.
Le système immunitaire est un réseau complexe de cellules et de composants
cellulaires, appelés molécules, qui travaillent normalement pour défendre
l'organisme et éliminer les infections causées par des bactéries, des virus et
d'autres microorganismes envahisseurs.
Le mot "auto" vient du
grec et signifie soi-même. Chez une personne atteinte d'une maladie
auto-immune, son système immunitaire attaque par erreur les cellules, les
tissus et les organes de son propre organisme.
Cela se produit lorsque le
système immunitaire fonctionne mal et que le corps ne fait pas la distinction
entre le sien et le corps étranger, modifie donc son bon fonctionnement et peut
mettre la vie en danger.
Le système immunitaire produit un
type de cellule qui sécrète des auto-anticorps pouvant se lier aux cellules et
aux tissus du corps. Chez les personnes ayant un système immunitaire en bonne
santé, plusieurs mécanismes contrôlent ces cellules et les expulsent du corps. Cependant,
le processus peut ne pas fonctionner correctement. Lorsque cela se produit, ces
cellules prolifèrent, produisant trop d'auto-anticorps, ce qui entraîne une
maladie auto-immune.
Ces auto-anticorps peuvent
endommager les articulations, le système digestif, le cœur, les poumons, les
reins, les nerfs, les follicules pileux, le tissu conjonctif de la peau et les
vaisseaux sanguins. Bien que chaque trouble soit différent, ils partagent
souvent des symptômes tels que fatigue, vertiges et fièvre basse. L'inflammation
est une caractéristique de chacun d'entre eux, à la fois sur le lieu de la
maladie, dans les articulations et dans le sang.
Parmi les maladies auto-immunes les
plus courantes, on trouve la polyarthrite rhumatoïde, qui s'attaque à la
muqueuse des articulations ; le diabète de type 1, qui détruit les
cellules nécessaires au contrôle du sucre dans le sang ; et la sclérose en
plaques, qui endommage la muqueuse nerveuse. Sont aussi présents la maladie de
Crohn, qui attaque le tractus gastro-intestinal ; la sclérodermie, qui provoque
la croissance anormale du tissu conjonctif de la peau et des vaisseaux sanguins ;
le psoriasis, dans lequel de nouvelles cellules cutanées sont endommagées ;
la maladie d’Hashimoto, qui affecte la glande thyroïde ; et le lupus érythémateux
systémique, pouvant endommager les articulations, la peau, le cœur, les poumons
et les reins.
Les maladies auto-immunes restent
un mystère pour la science. Jusqu'à présent, leurs symptômes et leur
développement sont connus, mais ce qui les produit est inconnu et la plupart
d'entre elles peuvent être traitées, mais non guéries. Il existe des hypothèses
à ce sujet, mais aucune d’elles n’est pleinement prouvée. Ce que l’on sait,
c’est que l'esprit joue un rôle important dans ces pathologies.
Ce qui est curieux à propos des
maladies auto-immunes, c’est qu’elles sont le résultat d’une attaque corporelle
contre le corps-même. L'organisme se comporte comme si ses propres antigènes étaient
des virus envahissants et les attaque. En d'autres termes, le système de
reconnaissance du propre et de l'étranger échoue. Cela se produit chez des
personnes en parfaite santé et la médecine ne sait toujours pas pourquoi.
Les interactions entre la
génétique et les premières expériences de la vie façonnent littéralement les
circuits du cerveau en développement, fortement influencé par l’harmonisation
ou non de ceux-ci, entre l’adulte et l’enfant, en particulier dans les
premières années de la vie. Les ajustements physiologiques et psychologiques à court
terme auxquels nous avons recours pour survivre dans cette première étape ont
des conséquences à long terme sur l'apprentissage, le comportement, la santé et
la longévité.
Les interactions entre le cerveau
et le corps déterminent également que des circonstances et des expériences
défavorables au cours de la petite enfance – même dans l'utérus – ont non
seulement des effets psychologiques à long terme, mais peuvent également être
des promoteurs de la maladie. De nombreuses études montrent que la souffrance
des premières années de la vie potentialise de nombreuses maladies, qu’elles
soient psychiques, telles que la dépression, la psychose ou l’addiction, aux
troubles auto-immuns et au cancer.
Les maladies auto-immunes
affectent davantage les femmes
Les femmes ont tendance à avoir
une réponse immunitaire plus forte que les hommes aux infections et aux vaccins
car elles produisent des taux plus élevés d’anticorps. Dans le cas de maladies
auto-immunes, ce trait semble contre-productif. "Une immunité solide chez
les femmes peut être bénéfique sur le plan évolutif, mais une immunité
excessive peut être mauvaise si elle est dirigée contre elles-mêmes", a
déclaré Rhonda Voskuhl, professeure de neurologie à l'Université de Californie
à Los Angeles, qui étudie la sclérose en plaques.
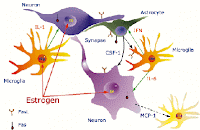
Les scientifiques pensent
également que les hormones sexuelles peuvent jouer un rôle important, car de
nombreux troubles auto-immuns surviennent chez les femmes peu après la puberté.
Certaines études indiquent en effet que les hormones féminines – œstrogène et
prolactine – stimulent la croissance des cellules produisant des anticorps. D'autre
part, la communauté scientifique estime également que les chromosomes sexuels,
en particulier le chromosome X, peuvent influer sur la propension.
Les symptômes de certaines
maladies auto-immunes, telles que le lupus, s'aggravent souvent pendant la
grossesse, alors que dans d'autres, telles que la polyarthrite rhumatoïde, ils
peuvent s'améliorer. Il n'est pas rare que les femmes aient leur premier
épisode de lupus pendant la grossesse. Il se serait probablement développé de
toute façon, mais cela a tendance à se produire pendant la grossesse.
La relation entre les maladies
auto-immunes et la ménopause est encore plus étroite. Il existe une certaine
incidence de femmes qui contractent une maladie auto-immune après la ménopause,
ce qui indique qu'il ne s'agit pas d'hormones.
Les maladies auto-immunes et les
mécanismes psychosomatiques
La science souligne que les
maladies auto-immunes résultent de multiples facteurs, parmi lesquels la
génétique joue un rôle important. Cependant, jusqu'à présent, il n'y a aucune
preuve concluante qu'il en soit ainsi. D'autre part, il a été prouvé que l'esprit
joue un rôle déterminant dans de telles pathologies, en particulier dans
l'expérience subjective qui produit la maladie.
Actuellement, les maladies
auto-immunes sont traitées par la plupart des professionnels comme des maladies
psychosomatiques. Cela signifie que ce sont des maux qui proviennent de
l'esprit et prennent forme à travers le corps.
Il existe différentes approches à
cet égard. Certains soutiennent que c'est une incapacité essentielle de
verbaliser ses émotions. D'autres indiquent qu'il s'agit d'une réponse
défensive contre la désintégration émotionnelle. Il s’agit également d’un “délire
corporel” dont l’antécédent est la dépression ou d’une réponse à un conflit
insoluble.
Quel que soit l'approche, la
vérité est que le point commun est la vérification de l’existence de réalités
dans l’esprit des gens et du fait qu’elles trouvent un moyen de se manifester par
le biais de la maladie dans le corps.
Les maladies auto-immunes sont
insidieuses et nuisent considérablement à la qualité de la vie. Elles sont
généralement douloureuses, difficiles à assimiler et sans espoir. Le pire,
c’est que ceux qui en souffrent se tournent vers le médecin pour obtenir des
réponses et, en général, ne trouvent que silence et palliatifs, pas toujours
efficaces, pour soulager leurs souffrances. Cependant, il est de plus en plus
clair que la santé et le bien-être sont des concepts intégraux, dans lesquels
le plan physique ainsi que le plan mental ont autant d'importance.
La sortie pour une personne
atteinte d'une maladie auto-immune est précisément de ne plus croire que c'est
une pilule, une vitamine ou un médecin miraculeux qui permettra de rétablir
leur santé. Ce n'est pas qu’elle ne devrait pas avoir recours à ces solutions,
mais que dans son traitement de base, il devrait y avoir l'intervention d'un
professionnel de la santé mentale.
Toutes les maladies comportent
une composante émotionnelle et mentale, mais dans les maladies auto-immunes, ce
facteur est absolument décisif. La résistance à traiter la maladie comme un
sujet de la psyché est certainement la raison fondamentale pour laquelle elles
ne trouvent pas de soulagement pour leurs souffrances physiques.
Une résistance qui découle de
l'idée erronée qu'une personne souffrant d'une maladie à base mentale est parce
qu'elle n'est pas assez forte et repose sur une idée encore plus fausse :
cette douleur est une invention du patient.
L'influence des émotions sur
les maladies auto-immunes
Les maladies auto-immunes mettent
en place un mécanisme d'autodestruction. C'est le corps lui-même qui cesse de
reconnaître les antigènes qui lui appartiennent et commence à s'auto-attaquer,
comme si ce qu'il transportait à l'intérieur était menaçant ou dangereux.
L'esprit est tellement important
dans ces processus qu'une nouvelle discipline est même apparue pour traiter ces
maux, connue sous le nom de psycho-neuro-immunologie. Ainsi, la vérité est que les
maladies auto-immunes sont non seulement chroniques, mais aussi elles sont
incapacitantes et peuvent conduire une personne à la mort.
Les études réalisées suggèrent
que les personnes atteintes de ce type de maladie présentent généralement un
niveau de dépression élevé, mais cela n’est pas toujours évident. Dit
autrement, il est possible qu'il s'agisse même de quelqu'un souriant et vital,
mais dans le fond il porte une grande insatisfaction que, en général, ni lui-même
reconnaît.
Une autre caractéristique
fréquente est une certaine incapacité à reconnaître ses émotions. Soit par une
intellectualisation excessive ou une rationalisation des situations, soit parce
qu’il s’agit de personnes qui veulent tout contrôler et qui ressentent les
affections comme une menace pour leur autonomie.
La psycho-neuro-immunologie
C'est une branche de la science
qui étudie les interrelations complexes entre le système nerveux central – qui
contrôle les processus biologiques et psychiques – et le système immunitaire. Elle
est basée sur l'étude des mécanismes d'interaction entre le cerveau et le
corps, c'est-à-dire entre les différents systèmes physiologiques responsables
de l'homéostasie : le système nerveux, le système immunitaire et le
système endocrinien.
Dans les parois de l'intestin
grêle, il existe de vastes réseaux de neurones, le système nerveux entérique. Ce
système entérique n'est pas seulement formé par les neurones qui recouvrent la
muqueuse intestinale, mais principalement par les cellules gliales. Ces
neurones sont également capables de synthétiser des hormones, des
neurotransmetteurs et d'autres produits chimiques.
Dans des conditions normales, à
l'exception des benzodiazépines endogènes – endorphines et enképhalines –, il
n'y a aucune preuve scientifique que ces neurotransmetteurs traversent la
barrière hémato-encéphalique. Ils ne devraient donc causer aucun effet au
niveau du système nerveux central. Cependant, des modifications de la perméabilité
de la barrière hémato-encéphalique, comme dans les cas de stress chronique, de
maladies inflammatoires cérébrales ou systémiques entraînant une augmentation
des cytokines, ou une forme de transport ou un mécanisme physico-chimique non
encore trouvé, leur permettraient de passer à travers, influençant ainsi les
fonctions du système nerveux central.
Indépendamment des communications
probables établies par les neurotransmetteurs synthétisés dans l'intestin, les
informations sensorielles du système digestif atteignent les noyaux
neuro-végétatifs du tronc cérébral, d'ici au thalamus – centre intégrateur de
toutes les informations sensibles – et enfin au cortex sensible. Le thalamus
est à son tour interconnecté avec les structures du système limbique – origine
des réponses émotionnelles – et également avec l'hypothalamus – siège des
instincts de survie primaires régulés par les systèmes neuro-végétatif et neuro-hormonal
(neuro-axe hypothalamus-hypophysaire) –. Ces centres supérieurs exercent une
inhibition descendante ou facilitent la modulation des fonctions digestives et
des réflexes (vomissements, défécation, etc).
Le système nerveux central et le
système nerveux entérique lui-même peuvent provoquer une sensibilisation du
système nerveux entérique, provoquant des déséquilibres au niveau des taux de
neurotransmetteurs, ce qui facilite l'apparition de dysfonctionnements
gastro-intestinaux, de pathologies inflammatoires intestinales, d'intolérances
alimentaires, de maladies auto-immunes. Les leucocytes possèdent des récepteurs
pour presque tous les neurotransmetteurs, en particulier pour la sérotonine et
la dopamine.
*
* *
Les scientifiques découvrent
un nouveau lien entre le cerveau et le système immunitaire
Une équipe de chercheurs de
l'école de médecine de l'Université de Virginie (UVA), dans le cadre d'une
étude publiée dans la revue Nature en juin 2015, a fait une découverte
qui, selon eux, pourrait changer les manuels scolaires : ils ont déterminé
que le cerveau est directement relié au système immunitaire par des vaisseaux
lymphatiques dont on ignorait jusqu'à présent l'existence.
Le fait que ces vaisseaux n’aient
pas été détectés à ce jour, malgré le fait que le système lymphatique – qui
contribue principalement à la formation et à l’activation du système
immunitaire – ait été minutieusement cartographié dans l’ensemble du corps, est
déjà surprenant. Oui, mais la véritable importance de la découverte réside dans
les effets qu'elle pourrait avoir sur l'étude et le traitement de maladies
neurologiques telles que l'autisme, la maladie d'Alzheimer ou la sclérose en
plaques.
Le cerveau est comme n'importe
quel autre tissu connecté au système immunitaire, dans ce cas par les vaisseaux
lymphatiques méningés. Les méninges sont les membranes qui tapissent le
cerveau. On pense que pour chaque maladie neurologique à composante
immunitaire, ces vaisseaux peuvent jouer un rôle important.
Cette découverte a été rendue
possible grâce au travail d'Antoine Louveau, un post-doctorant du laboratoire
Kipnis, qui a inventé une méthode ingénieuse pour visualiser les méninges du
cerveau d'une souris sans les détruire. Cela a permis de détecter les vaisseaux
au microscope. Les vaisseaux lymphatiques sont décrits dans les tissus du
cadavre d'une souris. Les vaisseaux lymphatiques complètent les vaisseaux
sanguins du corps, transportant les cellules immunitaires dans tout le corps
par le sang.
 |
Carte du système lymphatique: ancienne (à gauche)
et mise à jour (à droite) pour refléter la découverte |
Ces vaisseaux lymphatiques
cérébraux ont pu rester cachés tout ce temps car ils étaient bien cachés, car
ils suivent un vaisseau sanguin principal jusqu'aux seins, une zone difficile à
enregistrer en images.
Le microbiome intestinal est
séparé de la circulation sanguine par la muqueuse de l'intestin et du cerveau
par la barrière hémato-encéphalique. Mais au cours des vingt dernières années,
l’idée que le cerveau jouit d’une immunité privilégiée a été progressivement
démantelée. Des études ont montré que le cerveau interagissait avec le système
immunitaire périphérique, même de manière unique. Les cellules immunitaires, en
quelque sorte, circulent dans le cerveau et les antigènes normalement produits
par une réponse immunitaire vont du cerveau aux ganglions lymphatiques.
La présence inattendue de ces
vaisseaux lymphatiques soulève un grand nombre de questions auxquelles il faut
maintenant répondre, à la fois sur le fonctionnement du cerveau et sur les
maladies qui l’affectent. Par exemple, dans le cas de la maladie d'Alzheimer,
il y a une accumulation de grandes portions de protéines dans le cerveau. On
croit que celles-ci peuvent s'accumuler parce qu'elles ne sont pas efficacement
éliminées par les vaisseaux trouvés.
Ces conduits variant également
avec l'âge, le rôle qu'ils jouent dans le vieillissement constitue un autre
moyen d'explorer. En outre, d’autres maladies neurologiques, de l’autisme à la
sclérose en plaques, doivent maintenant être reconsidérées, à la lumière de la
présence de quelque chose qui, selon la science, n’existait pas.
Les maladies auto-immunes
augmentent avec le stress chronique
Des chercheurs de l'Université
Ben Gurion, dans une étude publiée dans le European Journal of
Immunology en mars 2014, ont montré le lien qui existe entre le stress
chronique et les maladies causées par le système immunitaire.
La recherche a été menée chez des
souris soumises à des situations de stress élevé. Compte tenu de cette
situation, les souris ont libéré des taux de gluco-corticoïdes supérieurs à la
normale, ce qui a entraîné un dysfonctionnement du système immunitaire. L'étude
a également révélé que ce processus se produit plus fréquemment chez les femmes
que chez les hommes, ce qui expliquerait, selon les scientifiques, le grand
nombre de femmes atteintes de maladies auto-immunes.
Le stress chronique, ainsi que
d'autres facteurs tels que la génétique et l'environnement, peuvent nuire au
fonctionnement du système immunitaire, ce qui est important car il régule sa
défense et l'empêche d'être attaqué. Ce mécanisme part du cerveau, de
l'hypothalamus. Les corticostéroïdes sont généralement utilisés dans le
traitement des maladies auto-immunes, mais cette étude a montré que, dans les
situations de stress, non seulement ils ne permettent pas de les guérir, mais
ils les renforcent également.
Une étude révèle de nouveaux
liens entre le microbiote intestinal et les maladies auto-immunes
Une recherche du CSIC (Conseil
supérieur des recherches scientifiques) d’Espagne, dans le cadre d’une
étude publié dans le journal mBIO en octobre 2014, a décrypté le profil
du microbiote intestinal chez les patients atteints de LES (lupus érythémateux
systémique).
Le lupus érythémateux systémique (LES)
est une maladie auto-immune chronique qui amène le système immunitaire à
attaquer par erreur les tissus sains du corps. Il peut affecter la peau, les
articulations, les reins, le cerveau ou d'autres organes.
Les résultats montrent un
déséquilibre dans le rapport entre les deux groupes de microorganismes les plus
abondants dans l'intestin humain – les bactéroïdes et les Firmicutes –, en faveur du premier, alors que la charge bactérienne et la diversité étaient
similaires entre les patients et le groupe témoin.
Pour cette étude, les chercheurs
ont comparé un groupe de 20 patients atteints de LES dans une région
géographique spécifique (Asturies) avec un groupe similaire de personnes en
bonne santé, en tenant compte de facteurs tels que l'âge, le sexe, les
médicaments et les antécédents médicaux. Le groupe avec LES comprenait des
personnes présentant une grande variété de symptômes, ce qui a permis d'établir
une série de corrélations entre le profil microbien et la pathologie.
Les chercheurs indiquent de plus
en plus que le microbiote pourrait avoir un impact sur les symptômes et la
progression de certaines maladies auto-immunes. Cependant, comment et pourquoi
de l'influence de cette communauté microbienne sur le LES reste incertaine.
Il est connu, par exemple, que le
profil microbien intestinal pourrait être modulé par le biais de schémas
alimentaires comme des interventions diététiques visant à favoriser
l'augmentation des populations microbiennes ayant une incidence sur la
symptomatologie du LES.
Des chercheurs trouvent
comment réduire l'intensité de la réponse immunitaire pour traiter les maladies
auto-immunes
Une étude réalisée par des
chercheurs du Salk Institute of Biological Studies à La Jolla (USA),
publiée dans le magazine Neuron en janvier 2017, montre que pour mettre
fin à la destruction du système immunitaire, il serait nécessaire d'inhiber une
enzyme appelée "escramblase 1 des phospholipides” (PLSCR1).
En général, le système
immunitaire reconnaît et agit rapidement contre une menace potentielle telle
que les cellules infectées par un virus. Cependant, en agissant sur PLSCR1, les
chercheurs ont été en mesure de protéger les cellules infectées des attaques
immunitaires et d'augmenter l'expression d'un virus génétiquement modifié jusqu'à
six mois, créant ainsi un potentiel de traitement à long terme plus durable.
 |
| Des virus guérisseurs |
Tous les virus ne sont pas
"mauvais". Par exemple, certains virus peuvent être utilisés par des chercheurs
avec un objectif thérapeutique, tels que la correction des déficiences du
matériel génétique des cellules ou la destruction des cellules cancéreuses.
Après des millions d'années
d'évolution, les virus se sont spécialisés à pénétrer les cellules et
à utiliser leurs mécanismes moléculaires à leur avantage. Un aspect dont
les scientifiques tirent parti ces dernières années pour manipuler ces virus et
les utiliser comme vecteurs pour transporter du matériel aux cellules, qu’il
s’agisse d’un gène – qui sera inséré dans l’ADN cellulaire – ou d’un médicament.
Mais thérapeutiques ou non, ce sont toujours des virus, ils seront donc
également suivis et attaqués par le système immunitaire.
Afin d'empêcher les cellules
immunitaires de s'attaquer à ces virus “guérisseurs” et de tirer parti de leurs
avantages, les auteurs ont axé leurs recherches sur la réponse immunitaire du
cerveau. Et pour ce faire, ils ont injecté un adénovirus génétiquement modifié
dans le cerveau d'un modèle animal – des souris – afin d'observer les signaux
émis par les cellules infectées et les cellules immunitaires et d'analyser les
protéines produites en réponse à l'infection.
Une fois infectée, la cellule
émet des signaux de détresse, en cas d'exposition dans sa membrane externe d'un
lipide appelé “phosphatidylsérine” qui attire les cellules immunitaires du
cerveau – la microglie –. La microglie évalue s’il faut isoler la cellule
infectée – ce qui présente un risque d’extension de l’infection aux cellules
environnantes – ou la détruire – ce qui peut poser problème étant donné que la
fonction de cette cellule cérébrale peut être très importante, et une fois
éliminée, elle ne régénère pas.
Ainsi, et afin de connaître les
détails de cette décision de la microglie, les auteurs ont modifié les niveaux
des protéines impliquées dans la communication – ou "signalisation" – intra et extra-cellulaire.
Les résultats ont montré que la
réduction des niveaux de PLSCR1 entraînait une grande variété de changements
dans la réponse immunitaire : les microglies étaient maintenues à une
distance prudente, mais sans intervention, et la production de cytokines – protéines
favorisant l'inflammation – était réduite, tout en convoquant plus de cellules
immunitaires à combattre.
La PLSCR1 agit en transportant la
phosphatidylsérine à l'extérieur de la membrane cellulaire, activant le signal
de détresse.
Les infections. Les résultats
ont également montré que les effets protecteurs de l'inhibition de PLSCR1
étaient maintenus pendant six mois, la période maximale atteinte jusqu'à
présent avec toute manipulation des protéines impliquées dans la réponse
immunitaire. Un aspect qui est très important étant donné que PLSCR1 n'est pas
exclusif au cerveau, mais se retrouve dans tout le corps. A tel point que les
auteurs pensent que, au-delà de la facilitation du transport des traitements par
les virus, les résultats pourraient être appliqués à d'autres troubles
inflammatoires. – comme les infections – et même aux maladies auto-immunes et pathologies
neurodégénératives – en cas d'Alzheimer –.
Il suffit d’imaginer la
possibilité de développer un médicament inhibiteur que le patient pourrait
prendre pour réduire l’excès d’inflammation, ce qui aurait un effet bénéfique
considérable sur un grand nombre de maladies.
* *
*
Influence de l'alimentation et
de la nutrition sur les maladies auto-immunes
Les problèmes auto-immuns ont une
forte prédisposition génétique, mais les déclencheurs peuvent être un excès de
soleil, des infections, des médicaments ou d’autres conditions – telles que la
grossesse – qui stressent le corps.
De plus en plus de preuves
indiquent que l’alimentation joue un rôle dans la prévention, le retardement ou
l’inversion des maladies auto-immunes déterminées génétiquement.
L’intestin étant un site
important de nombreuses interactions complexes contrôlant l’immunité, il s’agit
de la plus grande interface entre un individu et son environnement et offre
donc la plus grande exposition possible à la construction de micro-organismes
immuns et à toxines et allergènes. Nous sommes ce que nous mangeons. Cela
suggère un rôle important des probiotiques et des prébiotiques dans
l'auto-immunité.
Les régimes maternels pendant la
grossesse et l’allaitement ont également une influence sur les processus
auto-immune. L'allaitement apparaît comme un facteur potentiellement protecteur
pour la prévention des allergies et de la maladie cœliaque.
Au cours des dernières années, il
a été démontré le rôle important des facteurs spécifiques du régime alimentaire, tels que la
vitamine D, la vitamine A, le sélénium, le zinc, les acides gras oméga-2, les
probiotiques, la glutamine (un acide aminé) et les flavonoïdes (substances chimiques
de produits végétaux qui protègent contre les maladies) dans les maladies
auto-immunes. La carence en vitamine D a été associée à une auto-immunité
accrue et à une susceptibilité accrue aux infections. Les associations entre la
vitamine D et les maladies auto-immunes ont été confirmées dans la sclérose en
plaques et la polyarthrite rhumatoïde.
Des études récentes indiquent
également que la vitamine A est un immune-régulateur puissant et peut jouer un
rôle dans la prévention de l'inflammation intestinale et de l'auto-immunité. La
modification du régime a montré son plus grand effet bénéfique quand il
commence avant ou juste après le début de la maladie. Un apport alimentaire
optimal mais équilibré maintient une croissance saine et une vie sans maladie.
Carences nutritionnelles liées
aux maladies auto-immunes
Si nous souffrons de carences en éléments
nutritifs essentiels, notre système immunitaire risque de s'épuiser, d'attaquer
les propres tissus de l'organisme et de conduire à l'auto-immunité.
Vitamine D. Régule et
prévient l'auto-immunité en stimulant les lymphocytes T régulateurs,
responsables de la différenciation entre les envahisseurs dangereux et les
"propres" cellules. Lorsque la vitamine D favorise la promotion de
ces cellules, elle enseigne au système immunitaire à ne pas s’attaquer. La
vitamine D renforce également la capacité de lutter contre les infections
virales et bactériennes pouvant déclencher ou aggraver des affections
auto-immunes.
Oméga 3. Des études ont
montré que les huiles oméga-3 améliorent
l'activation des cellules B et sélectionnent la production d'anticorps, ce qui
peut réduire la réponse inflammatoire et aider le système immunitaire à
combattre les agents pathogènes.
Vitamines B. Les vitamines
B ne fournissent pas seulement de l'énergie à nos cellules. Elles contrôlent
également la fonction immunitaire, les hormones, l'humeur, le sommeil, les
nerfs, la circulation et la digestion. La vitamine B12, par exemple, est
compatible avec la production de globules blancs, composants essentiels du
système immunitaire.
Sélénium. Le sélénium est
peut-être un minéral peu connu, mais des études montrent qu’il est essentiel pour
réguler une réponse immunitaire excessive et une inflammation chronique dans
les maladies auto-immunes. C'est également un nutriment essentiel au bon
fonctionnement de la thyroïde. Des études ont montré que l'augmentation du
sélénium chez les patients atteints de thyroïde auto-immune diminue les anticorps
de la thyroïde.
Zinc. Le zinc affecte de
nombreux aspects du système immunitaire, de la barrière cutanée à la régulation
des gènes au sein des lymphocytes (un type de globule blanc). En fait, le zinc
est essentiel à la production de globules blancs et des études ont montré que
les personnes présentant une carence en zinc sont plus sensibles aux agents
pathogènes.
Magnésium. Le magnésium,
qui est important non seulement pour la fonction immunitaire mais également
pour la santé cardiaque, est un minéral que la plupart des gens ont
chroniquement faible en raison de leur stress élevé et de leur régime
alimentaire riche en sucre (le sucre réduit les niveaux de magnésium). Il a été
démontré qu'une carence en magnésium entraîne une augmentation de la production
de cytokines pro-inflammatoires, ce qui augmente le niveau global
d'inflammation et contribue à l'auto-immunité.
L’importance de maintenir un
environnement intestinal dans des conditions de santé optimales est
incontestable, car c’est là que réside ce système nerveux entérique et où
toutes les vitamines, acides aminés, acides gras essentiels, etc. viennent
d’être fabriqués, nécessaires à la synthèse des hormones, neurotransmetteurs,
enzymes, etc. essentiels pour une fonction physique et mentale correcte.
Plus d’études scientifiques, dans
le domaine de la psycho-neuro-immunologie, sont nécessaires concernant les
relations entre ces deux cerveaux, le rôle joué par la microflore intestinale,
la synthèse de neurotransmetteurs par ce système nerveux entérique et la
possibilité de traverser la barrière hématoencéphalique en tenant compte de
certaines circonstances physiques et chimiques de la même barrière
hémato-encéphalique ou même de neurotransmetteurs.